
Ensayos clínicos para la hemofilia
Este manual contiene información básica sobre los ensayos clínicos para la hemofilia. La FMH no se compromete en la práctica
Año: 2022
Idioma: Español
Autor(es): Federación mundial de hemofilia
Formato: Documento
Para que un fármaco se convierta en un tratamiento que los médicos puedan recetar, primero debe probarse en una serie de fases del ensayo clínico, y enseguida evaluarse y aprobarse por una agencia reguladora. Cada fase del ensayo clínico tiene un propósito, y estas avanzan en orden de la fase 1 a la fase 4.
La FMH no se compromete en la práctica de la medicina y en ningún caso recomienda un tratamiento particular para individuos específicos. Para el diagnóstico o consulta de un problema médico específico, la FMH recomienda que se ponga en contacto con su médico o con el centro de tratamiento local. Antes de administrar cualquier producto, la FMH insta a los pacientes a que comprueben las dosis con un médico o con el personal del centro de hemofilia, y a que consulten las instrucciones impresas de la compañía farmacéutica.
La FMH no promueve ningún producto farmacéutico en particular y cualquier mención de una marca comercial en esta presentación es estrictamente con fines educativos.

Este manual contiene información básica sobre los ensayos clínicos para la hemofilia. La FMH no se compromete en la práctica
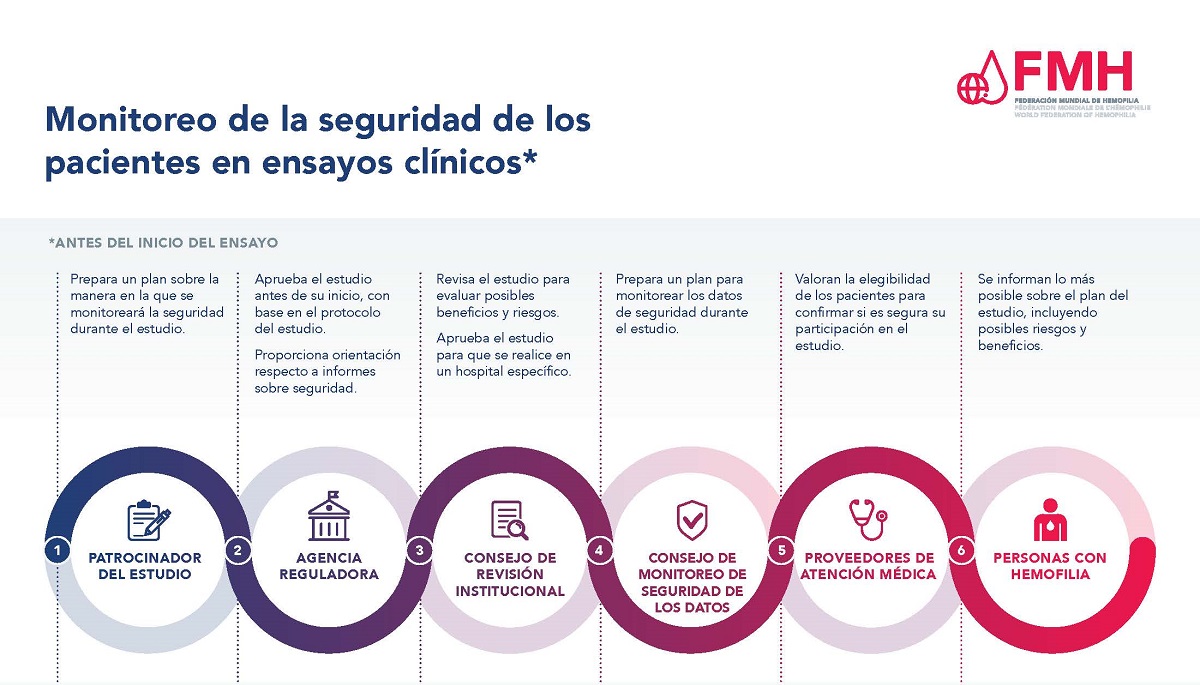
Garantizar la seguridad de los pacientes es de suma importancia durante el proceso del ensayo clínico. Hay muchos niveles de

Los participantes en los ensayos clínicos y los proveedores de atención médica tienen diferentes papeles a lo largo del proceso

Para las personas que están considerando participar en un ensayo clínico es sumamente importante aprender lo más posible sobre tal

Siga los avances de los estudios de terapia génica para la hemofilia con la Herramienta de ensayos clínicos en fase

Los ensayos clínicos deben satisfacer rigurosos estándares científicos y éticos. Esta monografía examina los principos básicos de la buena práctica