
Essais cliniques pour l’hémophilie
Ce manuel contient des informations de base sur les essais cliniques pour l’hémophilie. La Fédération mondiale de l’hémophilie ne pratique
Année: 2022
Langue: Français
Auteur(s): Fédération mondiale de l’hémophilie
Format: Document
Pour qu’un médicament puisse être prescrit par les médecins, il doit d’abord être testé au cours d’une série de phases d’essais cliniques, puis évalué et approuvé par un organisme de réglementation. Chacune des phases d’un essai clinique a un objectif bien spécifique et suit une chronologie de la phase 1 à la phase 4.
La Fédération mondiale de l’hémophilie ne pratique pas la médecine et ne recommande en aucun cas de traitement précis à qui que ce soit. Pour un diagnostic ou une consultation sur un problème médical spécifique, la FMH vous recommande de contacter votre médecin ou le centre de traitement local. Avant d’administrer tout produit, la FMH recommande aux patients de vérifier les doses avec un médecin ou le personnel du centre de traitement, et de consulter les instructions écrites fournies par le laboratoire pharmaceutique.
La FMH ne fait la promotion d’aucun produit pharmaceutique particulier et toute mention d’une marque commerciale dans cette présentation est strictement à des fins éducatives.

Ce manuel contient des informations de base sur les essais cliniques pour l’hémophilie. La Fédération mondiale de l’hémophilie ne pratique
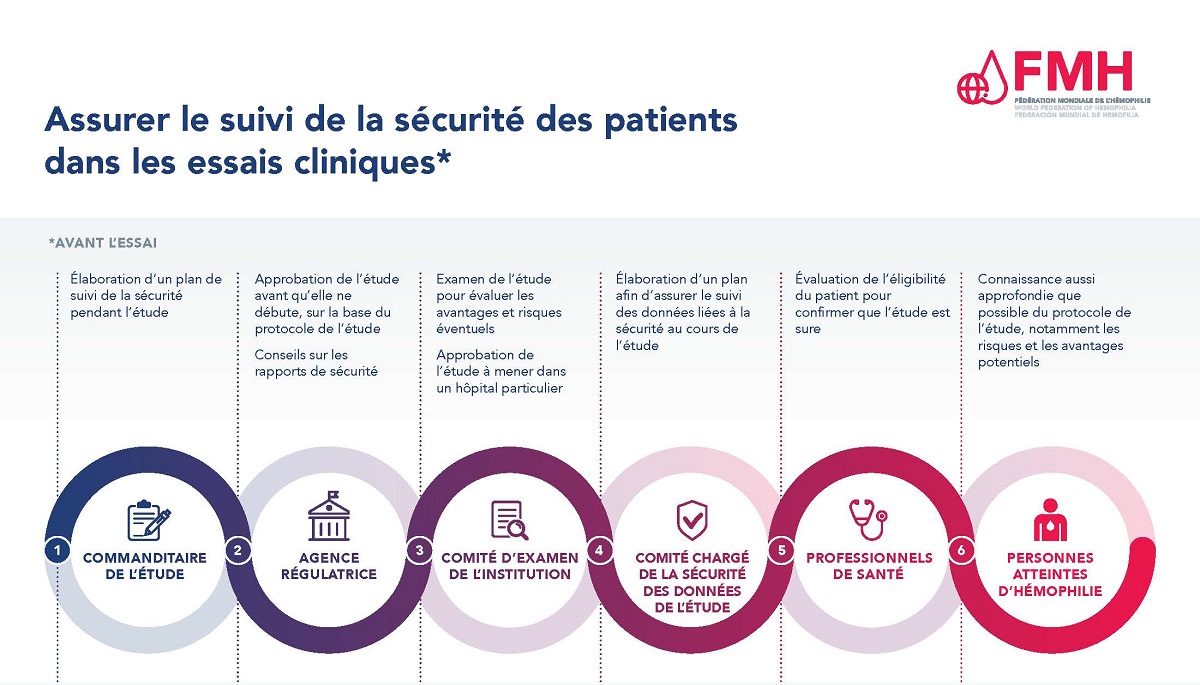
Assurer la sécurité des patients est d’une importance capitale au cours du processus d’essai clinique. Il existe de nombreux niveaux

Les participants aux essais cliniques et les professionnels de santé ont des rôles différents tout au long du processus d’essai

Pour les personnes qui envisagent de participer à un essai clinique, il est extrêmement important d’en apprendre le plus possible

Suivez l’évolution des essais cliniques en thérapie génique pour l’hémophilie et les recherches en cours grâce au Répertoire des essais